Когда правый не прав
У большинства населения диагноз «врожденный порок сердца» (ВПС) воспринимается как какое-то одно заболевание. Например, как ангина, грипп или понос.
Но это далеко не так, а количество разновидностей врожденной патологии сердца переваливает за сотню. Эти разнородные заболевания значительно разнятся между собой по причинам, изменениям внутренней структуры сердца и кровообращения в нем, степени сердечной недостаточности, а главное – по прогнозу жизни.
С некоторыми из пороков сердца, не леченых хирургически, можно дожить до старости, но большинство врожденных сердечных пороков требуют безотлагательного хирургического и поддерживающего терапевтического лечения. Есть и несовместимые с жизнью пороки.
Мало того, сложные пороки сердца зачастую ассоциируются с другими дефектами и аномалиями развития внутренних органов и систем организма, с хромосомными болезнями и синдромами, что еще больше усугубляет жизненный и социальный прогноз.
Никому из родителей не хочется услышать эти страшные слова: «У вашего ребенка порок сердца!» Но, к сожалению, традиционный менталитет «авось пронесет!» приводит к тому, что во время беременности сердце плода качественно не обследуется на УЗИ, всех удовлетворяет такое «подробное» его описание, как «без особенностей». А дальше, когда рождается ребенок с ВПС, начинается хождение по мукам.
Среди прочих пороков сердца, о которых мы уже не раз говорили, есть и синдром гипоплазии правых отделов сердца.
Этот вид патологии сердца относится к редко встречающимся врожденным порокам развития сердечно-сосудистой системы, его частота составляет около 2.5—5,6% среди всех врожденных пороков сердца, а соотношение мужчин и женщин с этим пороком 3 : 2 соответственно.
Суть этого порока заключается в недоразвитии и уменьшении объема правого желудочка, заращении, гипоплазии или стенозе устья легочной артерии и/или гипоплазии или атрезии (заращения) трехстворчатого клапана.
Возвращая Вас к началу нашей беседы, укажем, что и в этой разновидности порока сердца существует масса его вариантов — изолированная гипоплазия правого желудочка, стеноз легочной артерии с интактной межжелудочковой перегородкой, атрезия легочной артерии с интактной межжелудочковой перегородкой, атрезия трехстворчатого клапана с дефектом межжелудочковой перегородки, «верхом сидящий» трехстворчатый клапан, аномалия Уля (Uhl) правого желудочка, несбалансированная форма общего атриовентрикулярного канала и т.д.
Даже при клинически самом легком варианте этого порока редко кто больных живет дольше 30 лет, а у пациентов, у которых гипоплазия правого желудочка сочетается со стенозом легочной артерии и атрезией трикуспидального клапана, без хирургического лечения смерть наступает на первом году жизни, иногда – в первый месяц.
Приводим собственное наблюдение: беременность 17 недель, представлен вариант порока, характеризующийся наличием гипоплазии правого желудочка, атрезии трехстворчатого клапана (створки трехстворчатого клапана утолщены, спаяны и связаны короткими толстыми сухожильными нитями), сопутствующими дефектами межпредсердной и межжелудочковой перегородок, нормальным расположением магистральных сосудов, при этом нормально сформированы и функционируют морфологически левый желудочек, митральный клапан и аорта, однако устье легочной артерии гипоплазировано.
Что же делать пациенткам, у которых подозревается этот порок сердца плода:
1.Еще раз провести экспертное УЗИ сердца (ЭХОКГ) плода ( так как этот вид порока сердца относится к т.н. «трудным» для диагностики, высока вероятность неточностей и ошибок первичного диагноза). Требуется уточнить разновидность порока и его прогноз. Оптимальные сроки ЭХОКГ плода – 18-22 нед, однако наши статьи и наша практика демонстрируют возможности очень ранней – с 11 нед беременности – диагностики пороков сердца плода, чему могут позавидовать лучшие европейские клиники.
2.При подтверждении данного диагноза до наступления жизнеспособности плода обычно рекомендуют прерывание беременности, в других же случаях требуется уведомить родителей о возможном неблагоприятном прогнозе. При сохранении беременности необходима регулярное ЭХОКГ- исследование плода в целях своевременной диагностики у него сердечной недостаточности. Необходима дородовая консультация кардиохирурга, генетика, неонатолога. Родоразрешение проводят только в специализированных многопрофильных центрах, где возможно оказать экстренную кардиохирургическую помощь ребенку.
На фото и видео из собственной практики:
ЭХОКГ здорового плода: равные размеры желудочков сердца.
УЗИ сердца плода, 17 нед беременности. Гипоплазия правого желудочка, дефекты межжелудочковой и межпредсердной перегородок, атрезия трехстворчатого клапана.
Тот же случай. ЭХОКГ плода, режим ЦДК – отчетливо демонстрируется нормальный кровоток в левом желудочке, через митральный клапан, и отсутствие кровотока через атрезированный трехстворчатый клапан, кровонаполнение правого желудочка осуществляется через дефект межжелудочковой перегородки.
ЭХОКГ плода, режим ЦДК. ТВИ. 11 недель беременности. Симметричное кровонаполнение обоих желудочков сердца в норме
ЭХОКГ плода с синдромом гипоплазии правых отделов сердца:
на фоне нормальной функции митрального клапана отчетливо видно утолщение, уплотнение и отсутствие раскрытия створок трехстворчатого клапана, значительная асимметрия размеров желудочков: правый << левого, четко видны низкий дефект межпредсердной перегородки и высокий дефект межжелудочковой перегородки.
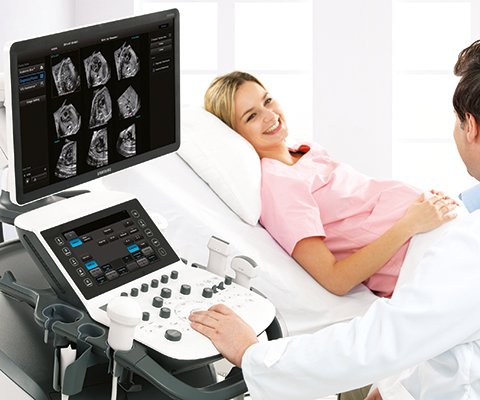
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Введение
За последние 20 лет прогресс новых медицинских технологий привел к появлению и бурному развитию такой области медицины, как ультразвуковая пренатальная диагностика. Разработаны и постоянно совершенствуются алгоритмы осмотра различных органов и систем плода, определены оптимальные сроки беременности для проведения скрининговых ультразвуковых осмотров. Достигнуты значительные успехи в диагностике некоторых врожденных заболеваний (например, болезни Дауна), а эффективность пренатального выявления отдельных пороков развития (например, анэнцефалии, кистозной гигромы шеи) достигает 100%. Тем не менее эффективность выявления такой важной группы заболеваний, как врожденные пороки сердца, все еще оставляет желать лучшего.
Пороки сердца являются наиболее распространенным врожденным заболеванием плода и занимают более 50% в структуре детской смертности, связанной с врожденной и наследственной патологией [1]. Несмотря на высокую разрешающую способность современной ультразвуковой аппаратуры, наличие цветового допплеровского картирования во всех современных аппаратах, частота выявления пороков сердца плода не превышает 40-45% [2]. В определенной степени такие скромные показатели связаны с небольшими размерами и сложной анатомией исследуемого объекта, а также с наличием динамических изменений, характерных для определенных пороков сердца плода, в связи с чем клиническая картина становится очевидной уже после 24 нед беременности. Однако в гораздо большем проценте случаев «пропуск» пороков сердца связан с нарушением методологии рутинного осмотра этого органа. Данная статья посвящена описанию наиболее распространенных ошибок, возникающих при рутинном осмотре сердца плода, и представляет методы оптимизации ультразвукового изображения при оценке основных сечений сердца.
Сечения, применяемые для рутинного осмотра сердца плода
Основным сечением, рекомендованным для проведения рутинного осмотра сердца плода, является четырехкамерный срез. Получение данного сечения не представляет сложностей и возможно при любом положении плода в более чем 95% случаев при проведении исследования после 19 нед беременности [3]. Однако существует ряд пороков, при которых четырехкамерный срез сердца остается неизменным, что делает недостаточным использование только этого среза для оценки сердца в ходе рутинного скринингового исследования плода. К порокам, при которых четырехкамерный срез сердца остается неизменным, относятся: тетрада Фалло, транспозиция магистральных артерий, общий артериальный ствол, двойной выход из правого желудочка, умеренный стеноз полулунных клапанов, аномалия дуги аорты, мелкие дефекты межжелудочковой перегородки (ДМЖП). В связи с низкой информативностью использования только четырехкамерного среза в настоящее время рекомендуется оценивать также срез через три сосуда и трахею, срез через выходные отделы левого желудочка («пятикамерный срез») и срез через выходные отделы правого желудочка. Критерии, которые используются для оценки основных срезов сердца, хорошо известны и описаны в отечественных справочных руководствах [4].
Оптимизация изображения сердца плода
При оценке любого из перечисленных сечений необходимо установить оптимальные настройки ультразвукового аппарата, чтобы добиться наилучшей визуализации исследуемого объекта. К сожалению, в большинстве клинических руководств по пренатальной ультразвуковой диагностике теме физических принципов получения ультразвукового изображения отводится крайне незначительное внимание. Это и приводит к недостаточной осведомленности врачей о физике ультразвукового исследования и неумению и даже боязни самостоятельно настроить ультразвуковой аппарат.
Наиболее распространенной и грубой ошибкой является оценка сердца плода в общем акушерском режиме. Почему так важно производить осмотр сердца плода в специальном режиме и какие принципиальные отличия данного режима от общего акушерского? Необходимо помнить, что сердце плода — это орган, который находится в постоянном движении, причем систола, диастола, движения клапанов происходят в 2 раза быстрее, чем в сердце взрослого человека. Чтобы получить более четкое ультразвуковое изображение движущегося органа, необходима высокая частота смены кадров. Частота смены кадров зависит от частоты датчика, которым производится осмотр, а также от угла развертки ультразвукового изображения. При использовании общего акушерского режима угол развертки изображения по умолчанию установлен на 60-65°, достигаемая при этом частота смены кадров является вполне достаточной для получения четкого изображения при осмотре большинства органов плода. Грудная клетка и сердце плода во II триместре беременности имеют небольшие размеры, для их визуализации вполне достаточно проводить сканирование при угле развертки изображения, равном 30°. При этом частота смены кадров увеличивается более чем в 2 раза. Примеры изображения сердца плода при использовании акушерского и сердечного режимов с различными углами развертки представлены на рис. 1.
Рис. 1. Изображения 4-камерного среза сердца плода. Беременность 22 недели и 1 день.
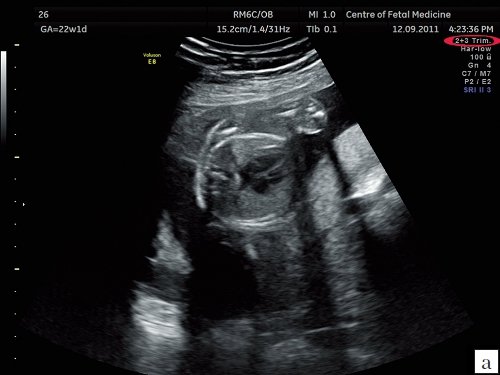
а) Эхограмма получена при сканировании в общем акушерском режиме. Обращает на себя внимание более широкий угол развертки изображения, контуры структур сердца более утолщенные и нечеткие по сравнению с изображением сердца в специальном сердечном режиме с узким углом развертки изображения.
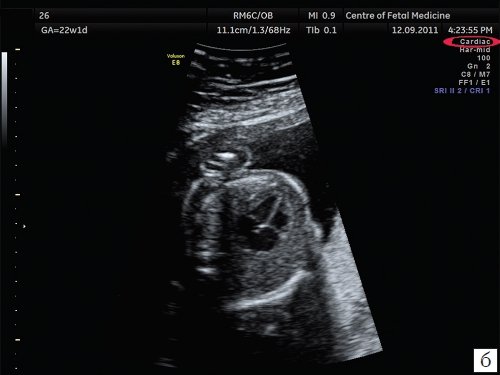
б) Эхограмма получена при сканировании в сердечном режиме. Контуры структур сердца более четкие, изображение более контрастное, по сравнению с изображением сердца на рис. 1a.
Второй наиболее распространенной ошибкой, которая имеет место при проведении ультразвукового исследования, является несоответствие расположения исследуемого органа и зоны фокусировки ультразвукового изображения. Данная ошибка характерна и для осмотра других органов и систем плода, но особенно значимо она сказывается при проведении осмотра сердца. Примеры изображения сердца одного и того же плода при различной глубине зоны фокусировки представлены на рис. 2.
Рис. 2. Изображения 4-камерного среза сердца плода при различной глубине зоны фокусировки. Беременность 22 недели и 1 день (то же наблюдение).
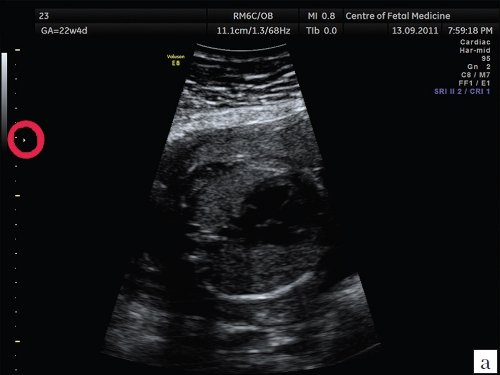
а) Зона фокусировки установлена выше исследуемого объекта.
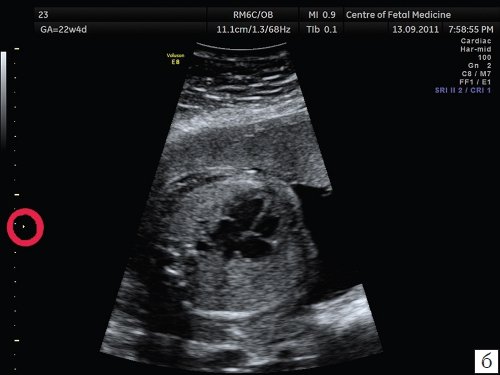
б) Зона фокусировки установлена на уровне исследуемого объекта.
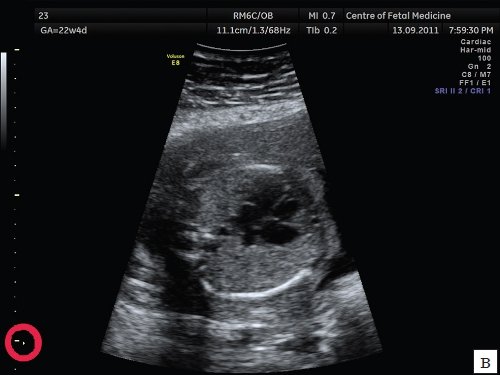
в) Зона фокусировки установлена ниже исследуемого объекта.
Описанные выше ошибки в настройке аппарата являются легко устранимыми и не требуют от оператора серьезных технических навыков, при этом четкость полученного изображения существенно возрастает. Возникновение следующей ошибки связано с выбором оптимального положения сердца плода для проведения осмотра. Достаточно часто врачи проводят осмотр сердца при субоптимальном его расположении, при этом часть исследуемого объекта не визуализируется в связи с наличием акустической тени от позвоночника, ребер или конечностей плода. Если осмотр сердца производится при наличии акустических теней от позвоночника, ребер или конечностей, то адекватная оценка предсердно-желудочкового соединения, межжелудочковой перегородки и кровотока в камерах сердца и магистральных сосудах значительно затруднена, что может приводить к «пропуску» порока сердца. Рекомендовано осуществлять осмотр сердца плода в таком его положении, чтобы верхушка сердца была направлена к датчику (на 11 и 13 ч). При исследовании сердца в положении верхушкой вниз осмотр области межжелудочковой перегородки, особенно ее мышечной части, затруднен, что увеличивает вероятность «пропуска» ее дефекта. Однако не обязательно дожидаться, чтобы плод сам принял положение «лицом к пупку матери»; смещение датчика по животу пациентки без изменения плоскости сканирования приведет к получению искомого изображения. При этом движения не должны носить хаотический характер, а осуществляться строго в ту сторону, куда направлена верхушка сердца плода (т.е. если верхушка сердца плода направлена к правому боку пациентки, то датчик смещается туда же и наоборот). Примеры изображения сердца одного и того же плода при смещении датчика показаны на рис. 3, 4.
Рис. 3. 4-камерный срез сердца при положении плода «спинкой кверху». Беременность 22 недели и 1 день (то же наблюдение).
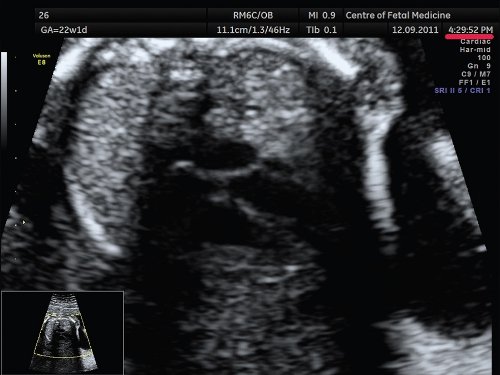
Акустическая тень от позвоночника перекрывает часть сердца.
Рис. 4. Оптимизация изображения 4-камерного среза сердца при положении плода «спинкой кверху». Беременность 22 недели и 1 день (то же наблюдение).
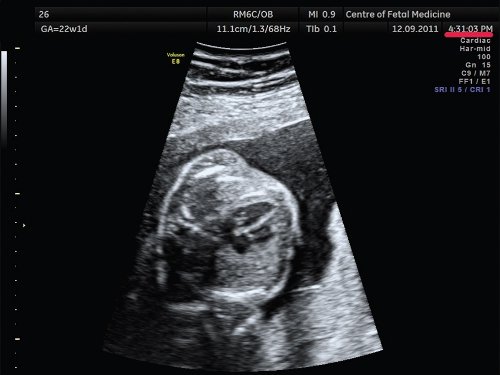
Смещение датчика к левому боку матери приводит к получению оптимального изображения 4-камерного среза сердца плода. Для оптимизации изображения сердца при положении плода «спинкой кверху» потребовалось чуть более 1 мин.
После получения изображения сердца плода верхушкой к датчику необходимо увеличить изображение таким образом, чтобы поперечное сечение грудной клетки плода занимало большую часть экрана. Строгое следование этому требованию связано с тем, что размеры сердца плода во II триместре составляют около 2 см и исследование такого маленького объекта требует максимального увеличения. Недопустимо проводить осмотр сердца без увеличения, так как при этом невозможно четко оценить межжелудочковую перегородку и область предсердно-желудочкового соединения. Многие современные ультразвуковые аппараты имеют возможность увеличения изображения уже после нажатия кнопки «freeze» (функция «post-freeze zoom»). Использование этой функции при проведении осмотра сердца недопустимо, так как в основе получения такого изображения лежит использование эффекта цифрового увеличения, т.е. изображение создается путем анализа информации от соседних пикселей (точек) и генерации новых пикселей, несущих усредненную информацию. Таким образом, полученное изображение сердца, несмотря на достаточные размеры, не будет нести никакой дополнительной диагностической информации; более того, контуры сердца будут более размытыми и нечеткими по сравнению с тем же изображением сердца без его увеличения.
В связи с этим единственным правильным способом увеличения изображения сердца является использование функции аппаратного увеличения («high definition zoom»). Выбор зоны для увеличения производится в режиме реального времени, все дальнейшее исследование происходит в реальном времени. На экране монитора ультразвукового аппарата появляется увеличенное изображение исследуемого органа, а в нижней части экрана возникает дополнительное изображение всей области сканирования с выделением той ее части, которая подверглась увеличению (рис. 5, а). Примеры изображения сердца одного и того же плода без увеличения и при использовании функции цифрового и аппаратного увеличения представлены на рис. 2, б и 5 а, б.
Рис. 5. Изображения 4-камерного среза сердца плода при использовании различных типов увеличения. Беременность 22 недели и 4 дня.
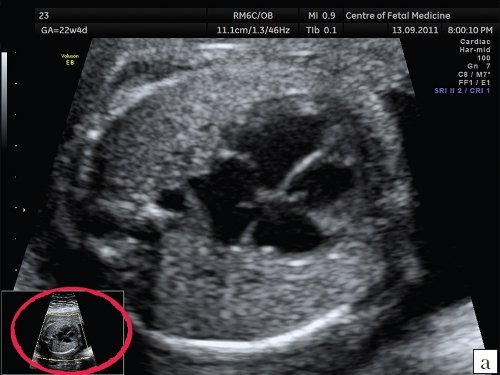
а) Увеличение изображения при помощи функции «high definition zoom».
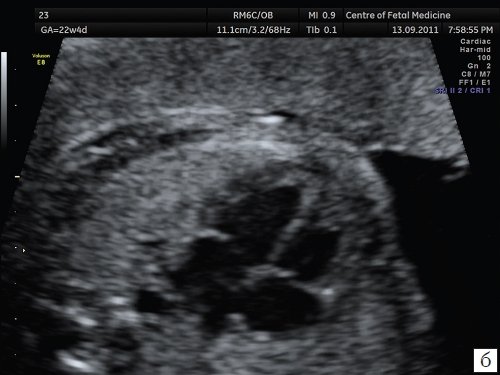
б) Увеличение изображения при помощи функции «post-freeze zoom».
Еще одной распространенной ошибкой при осмотре сердца плода является анализ изображения в реальном времени без использования кинопетли. Как уже было сказано выше, сердце плода — это орган, совершающий движения с частотой около 140-150 ударов в минуту. Таким образом, открытие и закрытие створок клапанов, сокращение и расслабление камер сердца происходят в интервал времени менее 1 с. Зрительный анализатор человека не способен адекватно оценить информацию, которая поступает к нему с такой быстротой. Именно поэтому оценка основных диагностических срезов должна проводиться не в одиночном изображении, а в нескольких сердечных циклах, полученных в одной кинопетле. При этом каждый кадр полученной кинопетли рассматривается с применением всех критериев оценки данного диагностического среза.
Согласно существующим отечественным рекомендациям, рутинное скрининговое исследование сердца плода во II триместре беременности выполняется с использованием только В-режима. Однако следует отметить, что использование режима цветового допплеровского картирования существенно увеличивает информативность исследования сердца плода, во многих странах Западной Европы и США в настоящее время рекомендуется использовать цветовой допплер при каждом осмотре сердца плода. Нежелание отечественных специалистов использовать цветовое допплеровское картирование во многом связано с неумением менять настройки этого режима; в полученном изображении цветовые сигналы «заливают» изображение камер сердца и перегородок, проводить анализ такого изображения невозможно. Для преодоления этих ошибок необходимо помнить несколько простых правил, которые приведены ниже.
Во-первых, осмотр сердца плода с использованием режима цветового допплера должен проводиться при определенных показателях скоростной шкалы, причем для осмотра различных отделов сердца эти показатели должны меняться. Регулировать показатели скоростной шкалы можно путем изменения частоты повторения импульсов (функция «pulse repetition frequensy» — PRF). Так, оценка камер сердца, атриовентрикулярных клапанов, полулунных клапанов, магистральных артерий производится при высоких значениях скоростной шкалы (более 35 см/с) (рис. 6). Использование более низких значений скоростной шкалы приведет к появлению «алайзинг-эффекта» и создает ложное впечатление о наличии турбулентного кровотока в камерах сердца.
Рис. 6. 4-камерный срез сердца плода, режим ЦДК. Беременность 22 недели и 1 день.
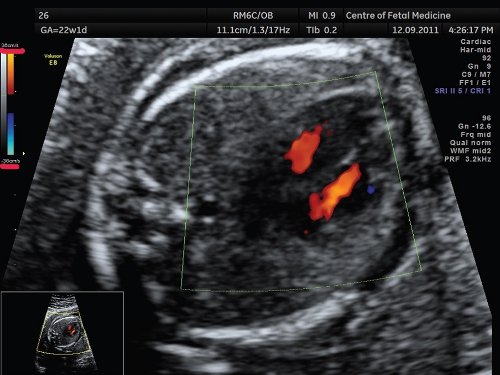
Значения скоростной шкалы установлены на 38 см/с, что позволяет получить изображение ламинарного тока крови в желудочках.
Кровоток в полых и легочных венах, напротив, характеризуется низкой скоростью, поэтому их оценка должна проводиться при низких значениях скоростной шкалы (10-20 см/с). Если проводить осмотр полых или легочных вен при том же значении скоростной шкалы, что использовалось для оценки камер сердца и магистральных артерий, то цветовой сигнал от них может отсутствовать.
Исходя из этого же принципа, необходимо менять значения цветового фильтра, который позволяет исключить сигналы от движения стенок и другие низкоскоростные сигналы. При оценке отделов сердца, в которых кровоток имеет высокую скорость, необходимо устанавливать высокие значения цветового фильтра, тогда как при исследовании полых и легочных вен необходимо пользоваться низкими значениями фильтра.
Во-вторых, при осмотре сердца в режиме ЦДК необходимо правильно выбрать размер цветового окна, так как при больших его размерах частота смены кадров существенно снижается, что приводит к получению менее четкого изображения. В связи с этим необходимо ограничивать размеры цветового окна границами сердца и крупных сосудов. Недопустимо, чтобы размер цветового окна занимал всю область сканирования, так как полученное при этом изображение будет очень размытым. Частота смены кадров не будет достаточной для регистрации всех изменений на протяжении одного сердечного цикла, и при исследовании в режиме реального времени это будет приводить к возникновению изображения с высокой степенью кадрированности, т.е. не плавного перехода систолы в диастолу, а прерывистой регистрации отдельных фаз сердечного цикла.
В-третьих, при оценке сердца в режиме ЦДК достаточно часто возникает необходимость изменить усиление (gain) цветового сигнала, как правило, в сторону его уменьшения. Осмотр сердца плода при высоких значениях усиления цветового сигнала является самой распространенной ошибкой, приводящей к появлению артефактов в виде наложения цветового сигнала на границы исследуемых структур, например, на межжелудочковую перегородку, приводя исследователя к ложному впечатлению о наличии ее дефекта (рис. 7). Необходимо начинать осмотр сердца при низких значениях усиления цветового сигнала, постепенно увеличивая их до достижения оптимальной картины.
Рис. 7. 4-камерный срез сердца плода, режим ЦДК. Беременность 22 недели и 4 дня.
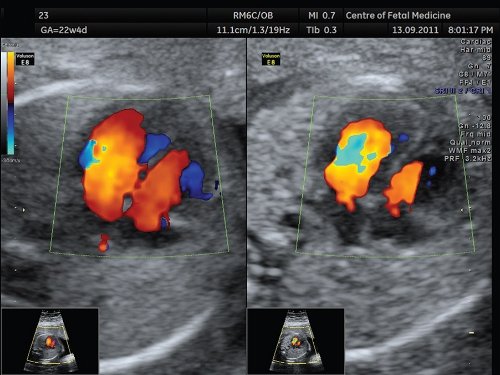
В левой части экрана представлено изображение с высоким усилением цветового сигнала. Обращает на себя внимание наложение цветового сигнала на межжелудочковую перегородку, что не позволяет адекватно оценить ее целостность. Справа — изображение, сбалансированное по силе цветового сигнала. Отмечается отсутствие кровотока через межжелудочковую перегородку.
Последнее, но немаловажное правило при использовании режима ЦДК — правильный выбор угла инсонации. С помощью допплеровского исследования можно оценить скорость и направление движения крови в камерах сердца и сосудах. Цветовой сигнал является отображением вектора скорости кровотока; характеристики цветового сигнала будут меняться в зависимости от положения сердца плода по отношению к ультразвуковому датчику. Если верхушка сердца плода направлена на 9 или 15 ч по отношению к датчику, то цветовой сигнал от камер сердца может отсутствовать, так как направление тока крови в них будет перпендикулярно движению ультразвуковой волны. При положении верхушки сердца на 11-13 ч направление тока крови в камерах сердца будет соответствовать направлению движения ультразвуковой волны и цветовой сигнал от камер сердца будет достигать максимальной интенсивности и иметь красное окрашивание. При положении верхушки сердца на 17-19 ч вектор тока крови также соответствует вектору движе ния ультразвуковой волны, но цветовой сигнал будет иметь синее окрашивание. Такой же принцип необходимо применять при оценке кровотока в магистральных сосудах — цветовой сигнал в них будет меняться в зависимости от положения сердца.
Заключение
Описанные в настоящей статье правила настройки аппарата, без сомнения, не являются гарантом успеха при диагностике пороков сердца плода. Для успешного осмотра сердца необходимо глубокое знание нормальной и патологической анатомии сердца плода и тех динамических изменений, которые имеют местопри беременности. Тем не менее строгое следование всем правилам настройки аппарата при каждом осмотре сердца плода существенно улучшает условия визуализации и способствует выявлению даже небольших отклонений от нормальной ультразвуковой картины этого органа.
Литература
- Hoffman J.I.E., Christianson R. Congenital heart disease in a cohort of 19502 births with long-term follow-up // Am. J. Cardiol. 1978. V. 42. P. 641.
- Tegnander E., Williams W., Johanses O.J. et at. Prenatal detection of heart defect in a non-selected population of 30, 149 fetuses — detection rates and outcome // Ultrasound Obstet. Gynecol. 2006. V. 27. P. 252-265.
- Shultz S.M., Pretorius D.H., Budorick N.E. Fourchamber view of the fetal heart: demonstration related to menstrual age // J. Ultrasound Med. 1994. V. 13. P. 285-289.
- Основные плоскости сканирования и дифференциально-диагностические критерии // Врожденные пороки сердца и главных артерий // Пренатальная эхография / Под ред. Медведева М.В. М.: Реал Тайм, 2009. С. 137-150.
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Если вашему ребенку поставили диагноз врожденный порок сердца, не стоит опускать руки, нужно узнать все способы поддержания здоровья таких детей, а также причины развития данного заболевания, пройти необходимое обследование, чтобы врач назначил соответствующее лечение.
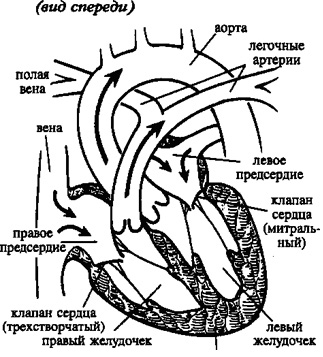
Сердце человека состоит из четырех камер: правое предсердие (ПП) и правый желудочек (ПЖ), левое предсердие (ЛП) и левый желудочек (ЛЖ). Правые и левые отделы сердца между собой никак не сообщаются. В этом нет необходимости, так как они обеспечивают движение крови каждый по своему кругу. Левые отделы сердца отвечают за движение крови по большому кругу кровообращения. Из левого предсердия через левый желудочек в аорту (Ао) поступает артериальная кровь, богатая кислородом. Из аорты по многочисленным артериям, а потом и по капиллярам она разносится по всему организму, доставляя клеткам кислород. В свою очередь, «отработанная» организмом венозная кровь собирается в мелкие вены, которые сливаются в более крупные венозные сосуды – верхнюю и нижнюю полые вены (ВПВ и НПВ). Конечная точка путешествия венозной крови – правое предсердие. Оттуда через правый желудочек кровь попадает в легочную артерию (ЛА). Малый круг кровообращения проходит через легкие, где венозная кровь обогащается кислородом и вновь становится артериальной. Отток обновленной крови осуществляется по легочным венам (ЛВ), впадающим, в свою очередь, в левое предсердие.
Особенности кровообращения у плода и новорожденного
Находясь в утробе матери, плод не дышит самостоятельно и его легкие не функционируют. Кровообращение осуществляется через плаценту. Насыщенная кислородом кровь матери поступает к плоду через пуповину: в венозный проток, откуда через систему сосудов в правое предсердие. У плода между правым и левым предсердием имеется отверстие – овальное окно. Через него кровь попадает в левое предсердие, затем в левый желудочек, аорту – и ко всем органам плода. Малый круг кровообращения отключен. В легкие плода кровь поступает через артериальный проток – соединение между аортой и легочной артерией. Венозный проток, овальное окно и артериальный проток имеются только у плода. Они называются «фетальными сообщениями». Когда ребенок рождается и пуповину перевязывают, схема кровообращения радикально изменяется. С первым вдохом ребенка его легкие расправляются, давление в сосудах легких снижается, кровь притекает в легкие. Малый круг кровообращения начинает функционировать. Фетальные сообщения больше не нужны ребенку и постепенно закрываются (венозный проток – в течение первого месяца, артериальный проток и овальное окно – через два-три месяца). В некоторых случаях своевременного закрытия не происходит, тогда у ребенка диагностируют врожденный порок сердца (ВПС). Иногда при развитии плода возникает аномалия и ребенок рождается с анатомически измененными структурами сердца, что также считается врожденным пороком сердца. Из 1000 детей с врожденными пороками рождается 8-10, и эта цифра увеличивается в последние годы (развитие и совершенствование диагностики позволяет врачам чаще и точнее распознавать пороки сердца, в том числе, когда ребенок еще в утробе матери).
«Синие» и «бледные» пороки сердца
Аномалии могут быть очень разнообразными, наиболее часто встречающиеся имеют названия и объединяются в группы. Например, пороки разделяют на «синие» (при которых кожные покровы ребенка синюшные, «цианотичные») и «бледные» (кожные покровы бледные). Для жизни и развития ребенка более опасны «синие» пороки, при которых насыщение крови кислородом очень низкое. К «синим» порокам относятся Тетрада Фалло, транспозиция магистральных сосудов, атрезия легочной артерии. К «бледным» порокам относятся дефекты перегородок – межпредсердной, межжелудочковой. В некоторых случаях порок может частично компенсироваться за счет открытого артериального протока (в норме он закрывается, как только легкие ребенка расправляются с первым криком). Также у ребенка может недоразвиться клапан сердца – сформируется клапанный порок (наиболее часто, аортальный клапан или клапан легочной артерии).
Причины развития врожденного порока сердца
У плода формирование структур сердца происходит в первом триместре, на 2-8 неделе беременности. В этот период развиваются пороки, которые являются следствием наследственных генетических причин или воздействия неблагоприятных внешних факторов (например, инфекция или отравления). Иногда у ребенка имеется несколько пороков развития, в том числе и порок сердца. Риск рождения ребенка с врожденным пороком сердца очень высок, если:
— ранее у женщины были выкидыши или мертворожденные
— возраст женщины более 35 лет
— женщина во время беременности принимает алкоголь, психоактивные вещества (наркотики), курит
— в семье женщины есть история рождения детей с пороками или мертворождения
— женщина живет в экологически неблагоприятной местности (радиация, отравляющие вещества)
или работает на экологически неблагоприятном производстве
— во время беременности (особенно первые 2 месяца) женщина перенесла инфекционные, вирусные заболевания
— женщина принимала во время беременности лекарственные препараты
с тератогенным эффектом (приводящие к развитию уродств у плода) или
эндокринные препараты для сохранения беременности (гормоны).
Можно ли поставить диагноз ВПС у плода?
Возможность выявить у плода врожденный порок сердца существует, хотя ее нельзя назвать абсолютно информативной. Это зависит от многих причин, основные их которых — наличие высококлассной аппаратуры и квалифицированного специалиста, имеющего опыт перинатальной диагностики. Диагностика возможна начиная с 14-й недели беременности. Если при обследовании у плода выявляется аномалия развития, родителям сообщают о тяжести патологических изменений, возможностях лечения и о том, насколько будет ребенок жизнеспособен. Женщина может принять решение о прерывании беременности. Если есть надежда на успешные роды и лечение, женщина наблюдается у специалиста, роды принимают в специализированном роддоме (чаще всего женщине предлагают кесарево сечение).
Врожденный порок сердца у новорожденных
При рождении ребенка или в первые дни его жизни врачи могут заподозрить врожденный порок сердца.
На чем они основывают свои предположения?
— Шум в сердце. В первые несколько дней жизни ребенка шум в сердце нельзя расценивать как достоверный симптом врожденного порока сердца. Такого ребенка наблюдают, при сохранении шумов более 4-5 суток – обследуют. Само появление сердечного шума объясняется нарушением тока крови через сосуды и полости сердца (например, при наличии аномальных сужений, отверстий, резкой смены направления кровотока).
— синюшность кожных покровов (цианоз). В норме артериальная кровь богата кислородом и придает коже розовую окраску. Когда к артериальной крови примешивается бедная кислородом венозная кровь (в норме не происходит), кожа приобретает синюшный оттенок. В зависимости от типа порока цианоз может быть разной степени выраженности. Однако, врачам приходится уточнять причины цианоза, так как он может быть симптомом болезней органов дыхания и центральной нервной системы.
— проявления сердечной недостаточности. Сердце перекачивает кровь, работая как насос. Когда снижается насосная способность сердца, кровь начинает застаиваться в венозном русле, питание органов артериальной кровью снижается. Учащаются сердечные сокращения и дыхание, появляется увеличение печени и отечность, быстрая утомляемость и одышка. К сожалению, эти признаки очень трудно распознать у новорожденных. Высокая частота сердечных сокращений и дыхания наблюдается у маленьких детей в нормальном состоянии. Только при значительных отклонениях можно с достаточной уверенностью говорить о развитии у малыша сердечной недостаточности. Часто следствием развития сердечной недостаточности является спазм периферических сосудов, что проявляется похолоданием конечностей и кончика носа, их побледнением. Эти признаки помогают косвенно судить о недостаточности сердца.
— нарушения электрической функции сердца (сердечного ритма и проводимости), проявляющиеся аритмиями и, иногда, потерей сознания. Врач может услышать неровное сердцебиение при аускультации (выслушивании фонендоскопом) или увидеть на записи электрокардиограммы.
Как сами родители могут заподозрить у ребенка врожденный порок сердца?
Если порок сердца приводит к серьезным нарушениям гемодинамики (кровотока), как правило, его диагностируют уже в роддоме. При отсутствии выраженных проявлений ребенка могут выписать домой. Родители могут заметить, что малыш вялый, плохо сосет и часто срыгивает, во время кормления и при крике — синеет. Может проявиться выраженная тахикардия (частота сердечных сокращений выше 150 ударов в минуту). В этом случае нужно обязательно сообщить о жалобах педиатру и пройти специальные обследования.
Подтверждение диагноза врожденного порока сердца
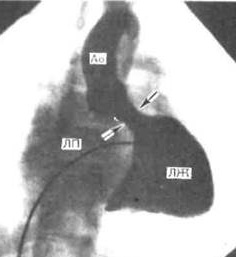
В настоящее время наиболее доступным, простым, безболезненным для ребенка и высокоинформативным методом диагностики пороков сердца является эхокардиография. Во время исследования с помощью ультразвукового датчика врач видит толщину стенок, размеры камер сердца, состояние клапанной системы и расположение крупных сосудов. Допплеровский датчик позволяет увидеть направления кровотока и измерить его скорость. Во время исследования можно выполнить снимки, подтверждающие заключение специалиста. Также ребенку обязательно запишут электрокардиограмму. При необходимости более точного исследования (как правило, для определения тактики хирургического лечения порока) врач порекомендует зондирование сердца. Это инвазивная методика, для выполнения которой ребенок госпитализируется в стационар. Зондирование проводится врачем-рентгенхирургом в рентгеноперационной, в присутствии врача-анестезиолога, под внутривенным наркозом. Через прокол в вене или артерии специальные катетеры вводятся в сердце и магистральные сосуды, позволяя точно измерить давление в полостях сердца, аорте, легочной артерии. Введение специального рентген-контрастного препарата позволяет получить точное изображение внутреннего строения сердца и крупных сосудов (см. рисунок).
Диагноз – не приговор. Лечение ВПС (врожденного порока сердца)
Современная медицина позволяет не только своевременно диагностировать, но и лечить врожденные пороки сердца. Лечением ВПС занимаются кардиохирурги. При выявлении порока, сопровождающегося серьезным нарушением гемодинамики, влияющего на развитие ребенка и угрожающего жизни малыша, операция проводиться как можно раньше, иногда в первые дни жизни ребенка. При пороках, которые не влияют значительно на рост и развитие ребенка, операция может проводиться позже. Выбор сроков операции определяется хирургом. Если ребенку рекомендовали хирургическое вмешательство и его не удалось выполнить своевременно (часто из-за отказа родителей, непонимания серьезности проблемы), у ребенка может начаться патологическое изменение гемодинамики, приводящее к развитию и прогрессированию сердечной недостаточности. На определенном этапе изменения становятся необратимыми, операция уже не поможет. Отнеситесь внимательно к советам и рекомендациям врачей, не лишайте своего ребенка возможности расти и развиваться, не быть инвалидом на всю жизнь!
Операция при врожденных пороках сердца
Многие годы операции при врожденных пороках сердца выполнялись только на открытом сердце, с использованием аппарата искусственного кровообращения (АИК), который берет на себя функции сердца во время его остановки. Сегодня при некоторых пороках такой операции существует альтернатива – устранение дефекта структур сердца с помощью системы AMPLATZER. Такие операции значительно безопаснее, не требуют раскрытия грудной клетки, не отличаясь по эффективности от «большой» хирургии. Если операция выполнена своевременно и успешно, ребенок полноценно развивается и растет, и часто – навсегда забывает о существовании порока. После операции обязательным является наблюдение педиатра, контрольные эхокардиографические исследования. Дети с врожденными пороками сердца часто болеют простудными заболеваниями из-за снижения иммунитета, поэтому в послеоперационном периоде проводится общеукрепляющее лечение и ограничиваются физические нагрузки. В дальнейшем у многих детей эти ограничения снимают и даже разрешают посещать спортивные секции.
Если Вы считаете, что у Вашего ребенка есть проблемы с сердцем, то Вы можете пройти эхокардиографическое исследование и обратиться за консультацией к детскому кардиологу.
Экстракардиальная патология у новорожденных как причина неверного диагноза врожденного порока сердца
Филиппова Е. А.1, Барышникова И. Ю.2
1НМИЦ АГиП им В.И. Кулакова, Москва; 2НМИЦ ССХ им. А.Н. Бакулева, Москва;
Актуальность. Причиной косвенных признаков ВПС — гипоксемии, кардиомегалии и легочной гипертензии (ЛГ) у новорожденных, могут быть не только ВПС, но и экстракардиальные врожденные пороки развития (ВПР). Наличие экстракардиальной патологии может кардинально повлиять на тактику терапевтического и хирургического лечения.
Цель исследования проанализировать спектр экстракардиальной ВПР, маскирующейся под ВПС и изучить возможности ультразвуковой диагностики в верификации диагноза.
Материал и методы. Ретроспективно были обследованы 2062 новорожденных, поступивших в НМИЦССХ из разных регионов России с первичным диагнозом ВПС, среди которых в 12 случаях выявлена изолированная экстракардиальная патология. У 5 пациентов, поступивших из НМИЦ АГиП им В. И. Кулакова, было верифицировано влияние экстракардиальной ВПР на появление клинических признаков недостаточности кровообращения и исключены ВПС. Всем пациентам выполняли ЭхоКГ исследование. При несоответствии клинической картины и ЭхоКГ данных повторно выполняли нейросонографию, ультразвуковое исследование органов брюшной. В случае стабильного состояния пациентов для исключения ВПС выполняли ангиокардиографию и компьютерную томографию с применением контрастного препарата (КТ-АГ).
Результаты. Из 4 случаев наличия аневризмы вены Галена, у 3 новорожденных пациентов сопутствующим диагнозом ошибочно была диагностирована коарктация аорты. У двух пациентов с высокой ЛГ и умеренной гипоксемией (SatO2=85-90%), при наличии преимущественно право-левого шунта крови через ООО, был установлен диагноз частичного аномального дренажа правых легочных вен. Последующее выполнение КТ АГ выявило нормальную анатомию легочных вен и наличие портокавального шунта (n=1) и большого аранцевого протока (n=1). В остальных 6 случаях у новорожденных присутствовала высокая ЛГ, обусловленная врожденной пневмонией и сопровождавшаяся выраженной гипоксемией, наличием право-левого шунта крови через ООО. В двух случаях состояние новорожденных было критическим — SatO2=28-33%% (FiO2-100%). Кровоток из легочных вен в левое предсердие не регистрировался. Терапия препаратами ПГЕ была неэффективна. Первичным диагнозом был установлен тотальный аномальный дренаж легочных вен. Ввиду критичности состояния и нетранспортабельности этим двум новорожденным была выполнена процедура закрытой атриосептостомии под контролем ЭхоКГ в условиях ОРИТ. Состояние было стабилизировано. Впоследствии, в возрасте 1,5 лет, одному их этих детей была выполнена пластика ДМПП.
Выводы: При наличии у новорожденных с сердечной недостаточностью изолированной экстракардиальной патологии ультразвуковая диагностика может быть достаточным инструментом постановки диагноза лишь при тщательном изучении анамнеза заболевания, грамотной трактовке клинических и лабораторных данных. Нетипичность клинической картины для подозреваемого порока является прямым указанием на необходимость дальнейшего обследования, несмотря на тяжесть состояния пациента.
Сердечные патологии сегодня лидирует в списке причин младенческой смертности. По данным статистики на одну тысячу новорожденных приходится примерно 8 случаев диагностированных пороков сердца. Но благодаря современным достижениям медицины, сегодня такой диагноз не является приговором. Даже самые сложные пороки успешно лечатся при условии, что патология обнаружена на ранних стадиях развития. Поэтому сегодня широко практикуется внутриутробная диагностика.
Особенности диагностики пороков сердца у плода
Первый ультразвуковой скрининг беременным женщинам проводится на сроках 11-13 недель. Процедура помогает выявить такие сложные пороки у плода, как:
- атрезия легочной артерии;
- отклонение сердечной оси;
- увеличенную толщин воротникового пространства;
- дефект межжелудочковой перегородки.
При детальном обследовании медикам удается выявить до 90% сердечных пороков именно с помощью внутриутробного обследования. Второе проведение скрининга на сроке 18-22 недели беременности уже дает более детальную картину имеющегося отклонения развития плода.
Самыми неблагоприятными считаются сложные пороки:
- аномальное отхождение магистральных сосудов;
- гипоплазия камер сердца;
- атрезии клапанов;
- наличие единственного желудочка.
Перечисленные аномалии развития не позволяют выполнить хирургическую коррекцию. Поэтому при таких пороках врачи дают неблагоприятный прогноз для жизни будущего ребенка.
Основная цель внутриутробной диагностики — сделать грамотный анализ течения беременности. При выявлении у плода кардиальной патологии врачу предстоит определить точность полученных диагностических данных с учетом развития других органов у плода.
Причины врожденных пороков
Вопреки устоявшемуся мнению, что врожденные пороки сердца имеют генетическую природу происхождения, такая связь обнаруживается в редких случаях. Намного чаще негативное влияние на формирующийся плод оказывают внешние факторы:
- вирусные инфекции: например, краснуха;
- хронические патологии у матери;
- алкоголизм и наркомания;
- ионизирующее излучение;
- прием некоторых лекарственных препаратов.
Но влияние на формирование пороков оказывает не только состояние здоровья матери, но и отца. К факторам риска также относится угроза прерывания беременности, мертворождение в анамнезе, а также наличие в семье детей с пороками развития. Конечно, даже на основе таких факторов невозможно дать точный прогноз, поэтому в подобных ситуациях родителей направляют на генетическую экспертизу.
Методы внутриутробной диагностики
На текущий момент тема перинатальной диагностики актуальна, как никогда ранее. Во многом такая тенденция объясняется информированностью населения. Ведь абсолютно всем родителям хочется иметь здоровое потомство. Особенно внимательно относятся к будущему материнству современные женщины, которые в большинстве своем четко выполняют все рекомендации гинеколога.
В свою очередь, главной задачей медиков является правильная тактика ведения беременности на всех этапах. После установки диагноза женщина находится под особым контролем, потому что достижения современной хирургии позволяют спасать жизни новорожденных с аномалиями развития. Выполненная в первые недели после рождения операция на сердце не отражается на качестве дальнейшей жизни.
К основным видам обследования в период беременности относятся:
- регулярное измерение артериального давления;
- контроль суточного баланса жидкости;
- биохимические анализы;
- ЭКГ;
- Электрокардиография.
Малышам сразу после появления на свет, если у них при внутриутробной диагностике был выявлен сердечный порок, назначаются инструментальные и лабораторные виды исследования, а также коагулограмма — комплексный тест крови. Также всем новорожденным проводится пульсометрия с обязательным измерением уровня сатурации. В случае необходимости детский кардиолог в Калининграде назначает рентгенографию органов грудной клетки.
Таким образом, диагностика пороков сердца в период внутриутробного развития плода является первой отправной точкой, от которой впоследствии можно отслеживать динамику состояния ребенка. При этом критические пороки сердца, которые нуждаются в срочном проведении хирургической операции составляют четверть от общего количества врожденных аномалий сердца.
С помощью фетальной эхокардиографии удается определить структуру этого порога, и составить прогноз для плода.
Результаты исследования
Здесь уместно отметить, что внутриутробный скрининг сегодня получил широкое распространение во всем мире. Такие мероприятия проводятся в детской многопрофильной поликлинике «Эдкарик». Поэтому все женщины, проживающие в Калининграде, могут пройти обследование, направленное на выявление пороков сердца у будущего ребенка.
К слову сказать, по последним данным статистики их 48 плодов со сложными пороками в 40 случаях патология была выявлена именно во время перинатальной диагностики. Каждая женщина имеет право сама решить, стоит ли ей рожать ребенка с крайне плохим прогнозом для жизни.
Сложность данного метода диагностики заключается в том, что неправильное положение плода может помешать проведению скрининга. Также осложняет процедуру многоводие и большой срок беременности (свыше 35 недель). Но подобные помехи осложняют ультразвуковое исследование и других органов плода, а не только сердечно-сосудистой системы.
И последнее замечание, на которое следует обратить внимание: проходить обследование во время беременности стоит лишь в учреждениях, имеющих лицензию на осуществление услуг такого рода. Работа частного детского центра «Эдкарик» подкреплена наличием всем необходимым разрешительных документов. Поэтому заключениям, сделанным нашими специалистами, можно доверять.
В качестве итога
Дородовая диагностика — это передовой метод исследования. С его помощью удается выявить у плода не только тяжелые пороки сердца, но также целый ряд других несовместимых с жизнью заболеваний. Например, синдром Дауна и Эдвардса сегодня тоже диагностируют еще на этапе гестации. Специалисты калининградской детской поликлиники «Эдкарик» обладают необходимыми знаниями и опытом, чтобы на качественном уровне выполнить весь комплекс диагностических процедур. Кроме высокого профессионализма наших детских кардиологов наших клиентов порадует:
- внимательное отношение персонала;
- полное отсутствие очередей;
- доброжелательная атмосфера в клинике;
- комфортные условия во время прохождения всех процедур.
Ко всему перечисленному можно добавить еще один существенный плюс — это вполне демократичные цены на все виды услуг.
После скрининга врач проанализирует полученные данные и сделает заключение. В случае выявления у плода порока сердца будет назначено повторное обследование. Узнать все подробности о проведении дородовой диагностики можно на официальном сайте нашего многопрофильного центра. Там же есть телефоны, по которым будущие мамы могут с нами связаться, чтобы выбрать удобное для обследования время. Мы ценим не только здоровье, но и время наших клиентов!